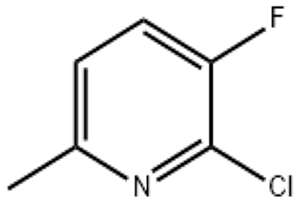
2-klor-3-fluor-6-pikolin (CAS-nr 374633-32-6)
Introduktion
Utseende: Vanligtvis färglös till ljusgul vätska, dessa utseendeegenskaper innebär att den kan vara känslig för ljus och värme, och det är nödvändigt att vidta åtgärder för att undvika ljus- och temperaturkontroll under lagring och transport, såsom att använda bruna glasflaskor och lagra dem i ett svalt lager för att förhindra ytterligare färgfördjupning och försämring.
Löslighet: Föreningen har god löslighet i vanliga organiska lösningsmedel, såsom toluen och diklormetan, följer principen om liknande löslighet och har en affinitet med organiska lösningsmedel på grund av den hydrofoba delen av molekylen; Lösligheten i vatten är dock låg, och den starka vätebindningen mellan vattenmolekyler är svår att effektivt brytas av molekylen, vilket gör det svårt att sprida den.
Kokpunkt och densitet: Kokpunktsdata är nära relaterade till dess flyktighet och kan ge nyckelparametrar för operationer som destillation och rening, men tyvärr har det specifika kokpunktsvärdet inte avslöjats i stor omfattning. Dess densitet är något högre än vatten, och att förstå densiteten kan hjälpa till att exakt uppskatta förhållandet mellan volym och massa omvandling i experimentella operationer eller industriella processer som vätskeöverföring och exakt mätning.
Kemiska egenskaper
Substitutionsreaktion: Kloratomen och fluoratomen i molekylen är de potentiella reaktiva platserna. I den nukleofila substitutionsreaktionen kan starka nukleofiler attackera de platser där klor- och fluoratomer finns, ersätta motsvarande atomer och generera nya pyridinderivat. Till exempel har det kombinerats med några kvävehaltiga och svavelinnehållande nukleofiler för att utveckla en serie kvävehaltiga heterocykliska föreningar med mer komplexa strukturer för läkemedelsupptäckt eller materialsyntes.
Redoxreaktion: pyridinringen i sig är relativt stabil, men när starka oxidanter, såsom kaliumpermanganat och väteperoxid paras med sura förhållanden, kan oxidation inträffa, vilket resulterar i förstörelse eller modifiering av pyridinringens struktur; Omvänt, med ett lämpligt reduktionsmedel, såsom metallhydrider, är det teoretiskt möjligt att hydrera intramolekylära omättade bindningar.
För det fjärde, syntesmetoden
Den vanliga syntesvägen är att utgå från enkla pyridinderivat och gradvis konstruera målstrukturen genom halogenerings- och fluoreringsreaktioner. Utgångsmaterialet pyridinföreningar metyleras först selektivt och metylgrupperna införs samtidigt; Använd sedan halogeneringsreagens, såsom klor och flytande klor, med lämpliga katalysatorer och reaktionsförhållanden, för att uppnå införandet av kloratomer; Slutligen användes fluorerade reagens, såsom Selectfluor, för att exakt fluorera målstället för att erhålla 2-klor-3-fluor-6-metylpyridin.
Används
Läkemedelssyntesintermediärer: dess unika struktur är älskad av medicinska kemister, och det är en högkvalitativ mellanprodukt för utveckling av nya antibakteriella, antivirala och antitumörläkemedel. De elektroniska egenskaperna och den rumsliga strukturen hos pyridinringar och deras substituenter kan specifikt binda till målproteiner in vivo och förväntas omvandlas till aktiva ingredienser med utmärkt effekt efter efterföljande modifiering i flera steg.
Materialvetenskap: Inom området för organisk materialsyntes kan den användas för att tillverka funktionella polymermaterial, fluorescerande material etc., tack vare sin förmåga att noggrant införa klor, fluoratomer och pyridinstrukturer, förse material med speciella elektriska och optiska egenskaper och främja utvecklingen av banbrytande teknologier som smarta material och displaymaterial.